
Lıtııdiń fızıkalyq jáne hımıalyq qasıetteri, ottekpen qosylystary
Ońtústik Qazaqstan obylysy
Shardara aýdany
№ 16 kolej
Oryndaǵan: Tu-43 top stýdenti Rysmurat Boldyqyz Muhtarqyzy
Jetekshisi: Aıtenova Nurgýl Ydyrysqyzy
Lıtıı - qalypty jaǵdaıda gaz tárizdi emes element.
Metaldyq lıtııdiń menshikti salmaǵy 0,534, sondyqtan ol benzınde de tutanady. Natrıı jóne kalıı sıaqty lıtıı álsiz sary túsi, metaldyq jyltyry bar, natrıı kalııge uqsas óte jumsaq.
Lıtııdiń normaldy potensıaly belgili potensıaldar ishindsgi teris mándi. Ol - 3,02 v-ke teń. Mundaı úlken teris potensıal máni lıtıı ıonynyń joǵary gıdratasıasymen baılanysty. Sondyqtan lıtııdi sýly eritindiden elektrolız arqyly bólý múmkin emes. Tuz balqymalarynda lıtıı potensıaly oń mándi — 2,1v. Alǵash ret metaldyq lıtııdi Devı lıtıı oksıdin vólt dińgegi arqyly ydyratý jolymen aldy, al keıinirek Býnzen men Mattısen balqytylǵan hlorıd elektrolızi arqyly aldy (1855 j.).
Lıtıı - tıptik metal, biraq basqa siltilik metaldardan erekshelenedi jáne magnıımen "dıagonaldar" erejesi boıynsha uqsastyǵy bar. Li+ jáne Mg2+ ıondyq radıýstary birdeı (0,78Aº). Lıtııdiń Mg-men uqsastyǵy onyń keıbir tuzdarynyń fosfat jáne karbonattarynyń óte az erigishtiginen baıqalady, lntıı basqa siltilik metaldarǵa qaraǵanda jáne magaııge uqsas ashýdas túze almaıdy. Bul qasıetteri lıtııli qosylysty óndirýde qoldanady.
Li basqa siltilik metaldarǵa qaraǵanda joǵary balqý temperatýrasyn kórsetedi jáne aýamen salystyrǵanda turaqtyraq. Biraq lıtıı metal túrinde qoldanylmaıdy, sebebi ol aýadaǵy azotpen Li3N túzedi. Basqa siltilik metaldarǵa sóıkes sýdy ydyratady, biraq natrıı men kalııge qaraǵanda jáne rýbıdıı men sezııge qaraǵanda azdap energıaly (balqymaıdy jáne jarqyly joq).
Lıtıı ftor jáne hlormen qalypty temperatýrada qosylady, sýtekpen qyzdyrǵanda gıdrıd LiN túzedi. Lıtıı qyzdyrǵanda kómirtek oksıdimen de árekettesedi.
Lıtııdiń osyndaı aktıvtiligine baılanysty bezın jáne parafın maıymen birge saqtaý kerek.
Súıytylǵan qyshqyldarda lıtıı tez erıdi, biraq konsentrli N2SO4 ony aqyryn eritedi, al konsentrli azot qyshqyly lıtııdi kúshti totyqtyratyny sonsha, ol balqyp sosyn Jalyndaıdy /1219/.
Ottekpen qosylystary
Lıtıı ottekte janǵanda aq totyq Li2O túziledi. Sonymen Li basqa siltilik metaldardan erekshelenedi, olar peroksıdti qosylystar beredi. Keıbir mólsheri Li2O2-niń lıtıı oksıdimen birige túziledi, biraq lıtıı peroksıdinin beriktigi, basqa siltilik metaldardyń peroksıdterine qaraǵanda joǵary emes: 195°S-ta ol tolyǵymen lıtıı oksıdine jáne ottekke ydyraıdy. Lıtıı oksıdiniń túzilý jylýy 142,3kkal/mol.
Lıtıı oksıdi ońaı, biraq basqa siltilik metaldar oksıdine qaraǵanda azdap energıaly, sýmen kelesi reaksıa boıynsha túziledi:
Li2O+N2O → 2LiON
Reaksıa kóp mólsherde jylý mólsheri bólinýi men júredi: Li oksıdiniń, gıdroksıdteriniń erigishtigi sýdaǵy (mol/l) basqa siltilik metal gıdroksıdterine qaraǵanda azdaý (150C).
|
LiOH |
5,3 |
RbOH |
17,9 |
|
NaOH |
26,4 |
CsOH |
25,8 |
|
KOH |
19,1 |
|
|
Sýly eritindilerden lıtıı gıdroksıdi bir molekýla sýy bar krıstalogıdrat túrinde krıstaldanady LiON · N2O.
Eger lıtıı gıdrooksıdin sýtek psroksıdimen óńdese, lıtııdsh peroksıdti qosylystaryn alýǵa bolady LiO2N2O2ZN2O, ony vakýmda keptirse sýsyz lıtıı peroksıdi túziledi; kuramy basqa peroksıdti qosylysta belgili - Li2O2-2N2O.
Ottekti qyshqyldyń tuzdary
Lıtııdiń túrli tuzdary lıtıı bar shıkiztty jáne lıtııdiń analıtıkalyq hımıasynda mańyzdy rol atqarady. Joǵarydaǵy keıbir tuzdardyń erigishtigi — karbonattar, fosfattar jáne basqalardyń - basqa siltilik metaldardyń sáıkes tuzdaryna qaraǵanda erekshelenedi, sondyqtan LiMg-ge jaqyn. Tuzdardyń erigishtigindegi mundaı aıyrmashylyq lıtııdi tabıǵatta birge kezdesetin siltilik metaldardan bólýge múmkindik beredi. 1 sýrette lıtıı súlfaty jáne karbonatynyń temperatýraǵa táýeldi erigishtigi berilgen, salystyrýǵa kalıı súlfatynyń erigishtiginiń qısyǵy berilgen. Kalıı karbonaty erigishtiginiń qısyǵy masshtabtyń shegine shyǵady, ony tómendegi sandardy qarastyryp onaı kórýge bolady:
|
Temperatýra, 0S |
0 |
10 |
20 |
25 |
30 |
100 |
|
Sýdyń erigishtigi g/100g |
||||||
|
Li2 CO3 |
1,53 |
1,42 |
1,33 |
1,27 |
1,18 |
0,66 |
|
K2 CO3 |
- |
109 |
110 |
- |
121 |
056 |
Na jáne K ıondary qatysynda jáne kómirtegi totyǵy qatysynda lıtıı karbonatynyń erigishtigi qos jáne kompleketi qosylystar túzilýi nátıjesinde ósedi. Lıtıı karbonaty siltide ońaı erıdi jáne lıtııdiń basqa tuzdaryn alýda shıkizat bolyp tabylady. Mysaly:
Li2SO3+2NS1 -> 2LiS1+N2O+SO2.
Lıtıı karbonaty óndirisindegi mańyzdy tuz bolyp tabylady, sebebi lıtııdi kenderden óndeý prosesi ony az erıtin karbonat túrinde tunbaǵa túsirýmen aıaqtalady.
1 sýretten korinip turǵandaı lıtıı súlfatynyń erigishtigi qalypty temperatýralarda kalıı súlfaty erigishtigine qaraǵanda joǵary jáne oǵan tek 100°S-da ǵana jaqyndaıdy, sondaı jaǵdaıda kalıı súlfaty erigishtigi joǵarylaıdy. Bul qasıet lıtıı kenderin óndeýde qoldanylady. Lıtıı basqa siltilik metaldarǵa qaraǵanda ashýdas túzbeıdi, natrıı, kalıı ne amonımen qos súlfat túzedi.
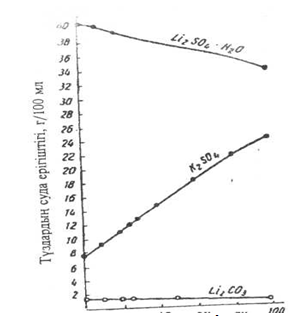
Temperatýra, 0
1 sýret - Lıtıı súlfaty men karbanatynyń temperatýraǵa baılanysty erigishtigi
Jaı súlfat eritindilerinen monogıdrat túrinde LiSO4 H2O krıstaldanady. Basqa krıstaldyq túrleri lıtıı súlfaty úshin belgisiz. Lıtıı basqa siltilik metaldrǵa uqsas tuz túzedi: LiHSO4, ol qyzydyrǵanda pırosýlfatqa aýysady LI2C2O; qalypty súlfattar natrıı, kalıı jáne basqa siltilik metaldardyń sýtek aǵynyna totyqsyzdaný múmkin nemese amıakty sýlfıtke deıin, totyqsyzdaný temperatýralary siltilik metaldyń sýlbfattry úshin birdeı (7000S – jýyq sýtek jine 8000S – jýyq amıak).
Li3PO4 lıtıı fosfaty 0,022g 100g sýda erıdi (00S – da), Na3PO4 erigishtigi 10,5g 100g sýda (150S), K3PO4 193,1g 100g sýda (250S).
Kremnıı qyshqyldyq lıtıı sýdý erimeıtin tuz, natrıı jine kalıı tuzdary jaqsy erıdi (suıyq shyny). Kremnıı qyshqyldyq lıtııdiń túzilýi tipti, metaldyq lıtııdiń kremnıı qyshqyldyq qosylystarmen árekettesýinde de ońaı ótedi. Bul jaǵdaı qaıta lıtııdiń balqýyn qıyndatady.
Ádebıetter tizimi:
1. Fersman A.E. Redkıe metaly. 1932, № 4-5.
2. Sajın N.P., Meerson G.A. Redkıe elementy v novoı tehnıke // Hım. naýka ı prom., 1956. T.İ, № 5.
3. Meerson G.A. ı Zelıkman A.N. Metalýrgıa redkıh metalov. Metıallýrgızdat, 1954.
4. Zelıkman A.N., Samsonov G.V., Kreın O.E. Metalýrgıa redkıh metalov. Metalýrgızdat, 1954.
5. Tronov V.G. Kklad rýsskıh ýchenyh v hımıý redkıh elementov. Izd. Znanıe, 1952.
6. Vınogradov A.P. Geohımıa redkıh ı rasseıannyh hımıcheskıh elementov v pochvah. Izd. AN SSSR, 1950.















